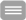Studienkonzept
Geeignete Patienten mit de novo BCR‐ABL positiver CML in chronischer Phase werden mit einem First‐Line TKI nach Wahl des behandelnden Arztes anbehandelt. Dabei sind vor TKI-Behandlung maximal 4 Wochen Behandlung mit Hydroxyurea erlaubt.
Patienten, die für weniger als 6 Wochen mit Nilotinib 300 mg BID, Imatinib 400 mg QD oder Dasatinib 100 mg QD behandelt werden, sind geeignet für den Studieneinschluss und werden der jeweiligen Kohorte (je maximal 30 Patienten) zugeordnet. Die Asciminib‐Therapie wird 12 Wochen nach Beginn von Nilotinib, Imatinib oder Dasatinib und nach Wiederherstellung der normalen Hämatopoese begonnen.
Nach 24 Monaten Therapie werden die Patienten auf der Grundlage ihres molekularen Ansprechens in Monat 24 drei Behandlungsarmen zugeteilt. Alle Patienten setzen die aktuelle Behandlung fort, bis die zugewiesene Therapie in Monat 25 begonnen wird.
Nach Monat 36 wird die Asciminib-Behandlung für alle Patienten beendet. Die weitere Behandlung hängt von der Aufrechterhaltung einer tiefen molekularen Remission (MR4 oder besser) ab: Patienten mit MR4 oder besser für mindestens ein Jahr werden die Behandlung beenden und in eine TFR-Phase eintreten. Das PCR-Follow-up wird gemäß den aktuellen Empfehlungen durchgeführt. Patienten, die eine MR4 verloren haben, werden nach Ermessen des Prüfarztes mit dem ATP-konkurrierenden TKI weiterbehandelt und nur hinsichtlich des Überlebens weiterverfolgt.